21. 取含有 Fe2O3 雜質的金塊樣品 3.2 克,以適量鹽酸使雜質恰完全作用,釋出的 Fe3+再以鐵還原成 Fe2+,該溶液中無 Fe3+殘留,其反應如式 1 及式 2。用去離子水將該溶液稀釋至 100毫升,取該稀釋液 10 毫升,在標準狀況下通入氯氣 13.44 毫升(視為理想氣體),可將 Fe2+完全氧化,如式 3 所示,該溶液中無 Fe2+殘留。試問金塊樣品中所含 Fe2O3 的重量百分比為多少?(Fe2O3 莫耳質量為 160 g/mol)
Fe2O3(s) + 6H+(aq) → 2Fe3+(aq) + 3H2O(l) (式 1)
Fe(s) + 2Fe3+(aq) → 3Fe2+(aq) (式 2)
2Fe2+(aq) + Cl2(g) → 2Fe3+(aq) + 2Cl−(aq) (式 3)
(A) 20%
(B) 30%
(C) 40%
(D) 50%
答案:登入後查看
統計: A(227), B(48), C(33), D(29), E(0) #3097966
統計: A(227), B(48), C(33), D(29), E(0) #3097966
詳解 (共 5 筆)
#6025522
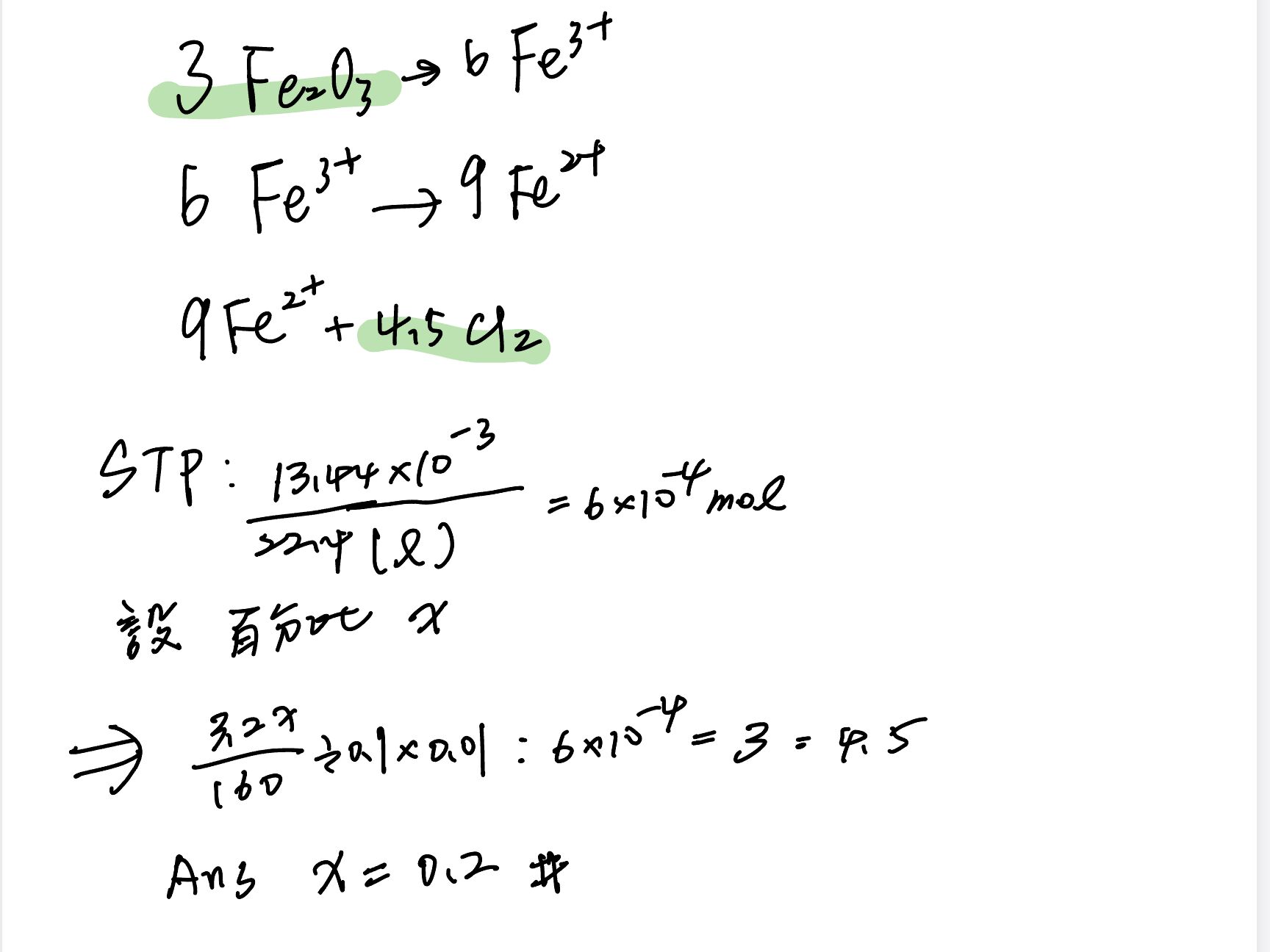
8
0
#7175054
[Fe氧化還原,計算重量百分比—相關考古題]
64. The iron in a 0.6656-g ore sample was reduced quantitatively to the +2 state and then titrated with 26.75 mL of the KMnO4 solution (0.02966 M). Calculate the percentage of Fe2O3 (Fe=55.8 g/mol) in the sample.
(A) 95.12 %
(B) 47.56 %
(C) 43.12 %
(D) 38.04 %
(E) 19.02 %
3
0