18-19為題組 一氧化氮和二氧化氮為常見的空氣汙染物。汽機車引擎的高溫可促使空..-阿摩線上測驗
載入中..請稍候..
18-19為題組
一氧化氮和二氧化氮為常見的空氣汙染物。汽機車引擎的高溫可促使空氣中的氮氣與 氧氣反應產生一氧化氮,一氧化氮再與空氣中的氧氣反應產生紅棕色二氧化氮,其反應 式如式(1)所示。兩分子的二氧化氮在密閉系統中可結合生成無色的四氧化二氮氣體, 其反應式如式(2)所示。
2NO(g)+ O2 (g)→NO2 (g) 式(1)
2NO2 (g)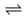 N2 O4 (g) 式(2)
N2 O4 (g) 式(2)
18. 在定溫下,式(1)反應物初濃度( [NO]0 、[O2 ] 0 )與生 成 NO2 之 初速率的關係如表 3
所示。下列相關敘述,哪些正確?

(A)反應物NO的反應級數為1
(B)反應物 O2 的反應級數為1
(C)此反應之速率常數 k 之數值為7000
(D)若 [NO]0 為0.030 M, [O2 ]0 為0.010 M,則
生成 NO2 之初速率為 6.3✖10-2 M/ s
(E)若要改善汽車排放廢氣汙染可加裝觸媒
轉化器,以加快生成 NO2 之速率
 | Kai 高一下 (2021/02/17): (A)首先比較實驗1、2的話,可以發現當NO濃度變為兩倍時,反應速率是變為原先的四倍的,因此可知速率對NO濃度呈現二次方正比關係。 (B)接著比較實驗1、3的話,可以發現當O2濃度變為兩倍時,反應速率是變為原先的兩倍的,因此可知速率對NO濃度呈現一次方正比關係。 (C)由AB選項可知此反應的速率定律式為r = k[NO]^2[O2] 因此若代實驗一的數據的話,可得知k=1.4✖10-2/[(0.01)^2*0.02]=7000 (D)r=7000*(0.03)^2*0.01=6.3✖10-2 M/s (E)觸媒轉化器會將氮的氧化物轉變回氮氣排出,並不會生成NO2 因此正確答案為BCD。 | 檢舉 |
|
|
|