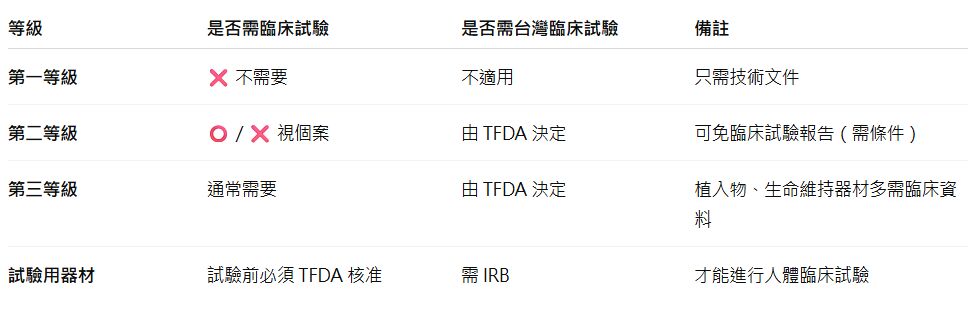
5.下列有關醫療器材臨床試驗之敘述,何者正確?
(A)申請查驗登記之醫療器材如係為第一等級者,應檢附臨床試驗報告
(B)申請查驗登記之醫療器材如係為第二等級且無類似品經中央衛生主管機關核准上市者,均免附臨床試驗報告
(C)申請第二等級或第三等級醫療器材查驗登記,應否在國內進行臨床試驗,另由中央衛生主管機關視申請之醫療
器材品項、個案及申請人檢送之資料核辦或公告
(D)試驗用醫療器材,應經中央衛生主管機關核准始得供經核可之區域醫院臨床試驗,以確認其安全與醫療效能
統計: A(2), B(2), C(2), D(1), E(0) #2897187
詳解 (共 1 筆)
(A) 「申請查驗登記之醫療器材如係為第一等級者,應檢附臨床試驗報告」
→ 錯誤。根據「醫療器材許可證核發與登錄及年度申報準則」及相關查驗登記準則,第一等級 (低風險) 的醫療器材登記所需文件主要是技術文件 (結構、材質、性能等),並不要求提供臨床試驗(或臨床試驗報告)。第一等級通常風險很低。實務上,不需要臨床試驗報告。也可參見 FDA 智慧醫療器材資訊平台 FAQ 說明。 aimd.fda.gov.tw
(B) 「申請查驗登記之醫療器材如係為第二等級且無類似品經中央衛生主管機關核准上市者,均免附臨床試驗報告」
→ 錯誤 (過度籠統)。雖然對於某些第二等級且無類似品 (no predicate) 的醫材,有「簡化規定」可免附整份臨床試驗報告,但不是「均免」臨床試驗報告。根據中央主管機關公告 (署授食字第 0991614012 號):「除中央主管機關另有公告需於國內進行臨床試驗者外 … 得免附臨床試驗報告資料」 衛生福利部食品藥物管理署+1
此外,必須符合一些條件 (例如預期效能無種族差異、適應症國外無嚴重不良反應、與國內已上市品不同處可以由臨床前資料佐證等) 官報電子版+1
所以說「均免」是不對的。
(C) 「申請第二等級或第三等級醫療器材查驗登記,應否在國內進行臨床試驗,另由中央衛生主管機關視申請之醫療器材品項、個案及申請人檢送之資料核辦或公告」
→ 正確。根據「醫療器材查驗登記審查準則」 (例如輸入第二、第三等級器材應檢具文件) 的規定:「申請查驗登記之醫療器材應否在國內進行臨床試驗,另由中央主管機關視申請之醫療器材品項、個案及申請人檢送之資料核辦或公告」。 衛生福利部食品藥物管理署
這表示是否要求國內臨床試驗,是由衛福部/TFDA (中央衛生主管機關) 個案評估、決定的。
(D) 「試驗用醫療器材,應經中央衛生主管機關核准始得供經核可之區域醫院臨床試驗,以確認其安全與醫療效能」
→ 部分正確但敘述不精確。確實,根據「醫療器材優良臨床試驗管理辦法」以及醫療器材管理法第 37 條,試驗用醫材在人體 (臨床試驗) 前必須經中央主管機關核准。 cde.org.tw+1
但敘述中說「供經核可之區域醫院臨床試驗」這樣表述不太準確:不一定限定「區域醫院」,而是 臨床試驗機構或試驗委託者 (可能是醫學中心或其他有資格的機構) 發起臨床試驗。再者,“以確認其安全與醫療效能”是試驗目的之一,但敘述「應經中央 … 始得供 … 臨床試驗」在語意上有點模糊。整體來看,比起 (C),(D) 的敘述較不精準。
結論
正確答案是 (C)。