題組內容
第二題:
城市供水系統從各種地點獲取水源,且這些水源在經由適當的處理後,作為自來水供民生工業所用。水源的來源包括地下水、地表水(湖泊和河流)以及經過淡化的海水等。水處理的步驟一般包括淨化、氯化消毒,有時還包括添加氟化劑。其中,氯離子(Cl-)含量的測量,在水源處理的步驟中特別重要。城市供水系統的氯離子含量測定一般是利用銀離子(Ag+)對水的樣品進行滴定。由於氯離子與銀離子結合會產生氯化銀沉澱,所以可以藉由銀離子滴定的量,經計算反推獲取該水樣品中氯離子的含量。其反應方程式如下,請回答下列問題:(未列出計算過程者不予計分)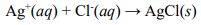
(一)若今有一水樣品,需使用 40.4 mL 的 0.100 M Ag+水溶液,才能將所有的氯離子沉澱出來,請問在該水樣 品中有多少克的氯離子?(氯的原子量為 35.5 g/mol)
(二)承第(一)小題,若該水樣品的質量為 10.0 g,其中包含了多少百分比的氯離子?【4 分】