試卷測驗 - 113 年 - 113 國立台灣師大附中學年度正式教師甄選試題:化學科#119240-阿摩線上測驗
lost剛剛做了阿摩測驗,考了11分
4.( )已知 R、Q、X、Y、Z 都是含有氯元素的化合物,其氧化還原反應如下:
(1) Q+H2O  X+H2; (2) R → Q+NaCl;
X+H2; (2) R → Q+NaCl;
(3) Y+NaOH → R+Q+H2O; (4) Z+NaOH → Q+X+H2O,
請由上述氧化還原反應推出在這五個化合物中,氯的氧化數由大到小之排列順序為何?
(A) X>Q>Z>Y>R
(B) Q>R>Y>Z>X
(C) X>Y>Z>R>Q
(D) Q>Y>R>X>Z
(E) X>Z>Q>Y>R。
 已知三個反應均能向右進行,試據此三個反應式,推測下列物質中哪一個是最強的還原劑?
已知三個反應均能向右進行,試據此三個反應式,推測下列物質中哪一個是最強的還原劑?
12. ( ) 在氯化鈉晶體中,兩個最近之鈉離子間的距離為  ,則氯化鈉的密度為多少 g/cm3?
,則氯化鈉的密度為多少 g/cm3?
(式量:NaCl=58.5)
(A) 1.08
(B) 1.45
(C) 2.17
(D) 3.26
(E) 4.36。
14. ( ) 在  的平衡系中,若測得壓力為 4 atm 時,平均分子量=55.2,則該反應的 Kp 為
何?(以 atm 為單位)
的平衡系中,若測得壓力為 4 atm 時,平均分子量=55.2,則該反應的 Kp 為
何?(以 atm 為單位)
(A) 1.6
(B) 3.6
(C) 6.4
(D) 12.8
(E) 16.4。
16. ( ) 反應:3A+B → 2C 中,根據實驗將結果製成圖表如附表和附圖(圖表中未出現的參數為控制變
因,r 為反應速率),則此反應之總級數為何? 
(A) 
(B) 1
(C) 
(D) 2
(E) 3。
17. ( ) 在 25 ℃ 時,設 Mg(OH)2 之 Ksp 值為 K1,Ca(OH)2 之 Ksp 值為 K2,同一燒杯中將上述兩種氫氧化物溶
於水,而達成飽和時,水溶液中 [OH-
] 為何值?(H2O 的解離忽略不計)
(A) 
(B) 
(C) 
(D)

(E)
 。
。
18. ( ) 一重量百分率濃度為 20%,密度為 1.2 克∕毫升的 A 物質水溶液 600 克,若其體積莫耳濃度為 2
M,則溶質 A 的分子量為何?
(A) 20
(B) 60
(C) 120
(D) 160
(E) 200。
19. ( ) 在 H2(g)+I2(g)  2HI(g)+17 kJ 平衡系中,以虛線畫出 HI 產量─時間變化圖如附圖,今改變下
列何項措施,可使 HI 產量─時間變化圖如實線描述?
2HI(g)+17 kJ 平衡系中,以虛線畫出 HI 產量─時間變化圖如附圖,今改變下
列何項措施,可使 HI 產量─時間變化圖如實線描述? 
(A)升高溫度
(B)降低溫度
(C)增加總壓
(D)加入鉑粉作為催化劑
(E)增加氫的分壓。
25.( )反應  ,則下列敘述何者正確?
,則下列敘述何者正確?
(A)若 1 莫耳 HNO3被還原,則實際消耗 1.6 莫耳 HNO3
(B)消耗 1 莫耳的硫化亞鐵,需消耗 5 莫耳
HNO3
(C)HNO3當氧化劑占 62.5%
(D)HNO3的當量為 21
(E)上述方程式之係數總和為 20。
27.( )於 25°C 下,有四個半電池 A—D,其中 A 與 B、C 與 D 分別以裝滿 1.0M NH4NO3溶液的鹽橋聯接如下
圖,各半電池的標準還原電位如下:

 下列敘述何者正確?
下列敘述何者正確?
(A)若將伏特計用導線連接於C 與D二半電池的電極所成的電池,理論上伏特計的讀數為0.57伏特
(B)承( A ),若燒杯中的銅離子的濃度由1.0M 減低為0.10M時,伏特計的讀數變小
(C)若將伏特計用導線連接於A與D 二半電池的鋅片與鎳片間,且以導線連接銀片與銅片形成一電池組,理論上
伏特計的讀數為0.99伏特
(D)承( C ),於C半電池燒杯中加入Na2S(aq),伏特計的讀數會變小
(E) 承( C ),此時Zn為陽極,Ni為正極。
28.( )某烴類之製備裝置如附圖,有關其性質的敘述,何者為正確? 
(A)水和電石反應生成黃綠色氣體為乙炔
(B)生成氣體與空氣的混合物,具有爆炸性,應嚴禁煙火
(C)此氣體可分別溶於 CCl4和 C2H5OH 中
(D)甲管溶液可使 Br2/CCl4溶液褪色,生成 1,1-二溴乙烯,證明生成氣體為不飽和烴
(E)乙管溶液可使 KMnO4溶液褪色,至呈褐色,生成乙二醇。
30.( )L-多巴胺是一種有機物,它可用於兒童和成人的腦神經病變的治療,其結構式如附圖,這種藥物的研製是基於獲得 2000 年諾貝爾 生理學或醫學獎和獲得 2001 年諾貝爾化學獎的研究成果。下列關於 L-多巴胺的敘述,何者正確?

(A)在鹽酸中的溶解度大於在純水中的溶解度
(B)在氫氧化鈉溶液中的溶解度大於在純水中的溶
解度
(C)可視為一種α-胺基酸
(D)和氯化鐵(Ⅲ)溶液混合則呈紫色
(E)可進行縮合聚合反應。
31.( )化學反應:aA(g)+bB(g)  cC(g)+dD(g),ΔH=-Q kJ,在不同溫度(T1 和 T2)及壓力(P1 和 P2)下,
產物 D 的莫耳數(nD)與反應時間(t)的關係如附圖所示,則下列哪些敘述正確?
cC(g)+dD(g),ΔH=-Q kJ,在不同溫度(T1 和 T2)及壓力(P1 和 P2)下,
產物 D 的莫耳數(nD)與反應時間(t)的關係如附圖所示,則下列哪些敘述正確? 
(A) T1>T2
(B) P2>P1
(C) Q<0
(D) a+b<c+d
(E) T2 , P1與 T2 , P2狀態下,所建立的平衡常數值,前者大於後者。
32. ( )取氫氧化鋇溶於 1 M NaOH 中製成飽和溶液後,取其澄清液與下列物質混合,則下列敘述何者正確?(氫氧化鋇之 Ksp=5.4 × 10-3)
(A)等體積 4 M NaOH 溶液混合時,即產生氫氧化鋇沉澱
(B)等體積 4 M NaOH 溶液混合時,即鋇離子濃度減低為原液之 
(C)等體積 4 M NaOH 溶液混合時,即鋇離子濃度變為
 Ksp
Ksp
(D)等體積水混合時,即鋇離子濃度變為  Ksp
Ksp
(E)等體積水混合時,即鋇離子濃度變為 4Ksp。
34. ( )萊克多巴胺(瘦肉精)結構如附圖,下列敘述何者正確? 
(A)以 sp
2 混成的原子個數為 12
(B)以 sp3 混成的原子個數為 10
(C)分子中所有 σ 鍵數目為 30
(D)分子中所有 π 鍵數目為 6
(E)孤對電子共有 7 對。
36. ( ) 一容積可變的容器內,在 27 ℃ 量得水蒸氣壓變化如附圖所示。在 1 升時,容器中再裝入 N2 氣體 600 mmHg,則下列哪些為正確的敘述?

(A)容器中水總量約為 0.26 克
(B) 15 升時總壓力為 58 mmHg
(C) 3 升時總壓力為 227 mmHg
(D) 3 升時液體水重約 0.18 克
(E)體積為 10 升以上時全部以氣體存在。
37. ( ) 一容器內裝理想氣體,以能自由滑動之活塞構成左、右兩室(如附圖)。在 27 ℃ 平衡時,左、右
兩室之體積均為 V。今將左室緩慢加熱至 127 ℃,右室保持原來溫度,則下列敘述,哪些正確? 
(A)原平衡時,左、右兩室壓力相等
(B)最後平衡時,左室氣體體積增加了 
(C)最後平衡時,右室氣體壓力增加了原來壓力的 
(D)最後平衡時,左、右兩室壓力仍相等
(E)體積改變過程,兩邊壓力必須維持相等。
39. ( ) 有關查理定律之敘述,下列哪些錯誤?
(A)適用於定壓下的定量氣體
(B)定壓、定量氣體之體積與溫度成反比
(C)定壓、定量氣體溫度每上升 1 ℃,體積增加為 30 ℃時體積的 
(D)定壓、定量氣體溫度由 27 ℃上升到 28 ℃
時,體積增加為 27 ℃時體積的 
(E)定壓、定量氣體溫度由 27 ℃上升到 28 ℃時,體積逸出
率為  。
。
40.( ) 同溫、同壓下,A 氣體 5 mL 和 B 氣體 1 mL 等重,且 A 氣體密度為 O2 的  ,
下列何者正確?
,
下列何者正確?
(A) A 分子量為 32
(B)密度 B>A
(C)擴散同體積的 A 氣體、B 氣體所需時間比為 1:

(D)同體積之兩種氣體所含分子數 A=B
(E)同重量之兩種氣體所含分子數:A>B。
4、琪琪欲使用碘量法檢驗市售的維他命 C(又稱抗壞血酸,ascorbic acid)錠中所含維他命 C 的含量。取
50mL0.01M 碘酸鉀溶液,置於 100mL 錐形瓶中,並加入 1.66g 碘化鉀(KI=166)與 25mL0.3M 硫酸,將溶
液稀釋至 100mL,配成所需的碘液。另取 0.2 克的維他命 C 錠磨碎後加水至 20mL,倒入錐形瓶中,並加入數滴 2%澱粉液。接著以碘液滴定維他命 C 溶液,達當量點時,用去碘液 10mL。已知下列反應式,回答各問題: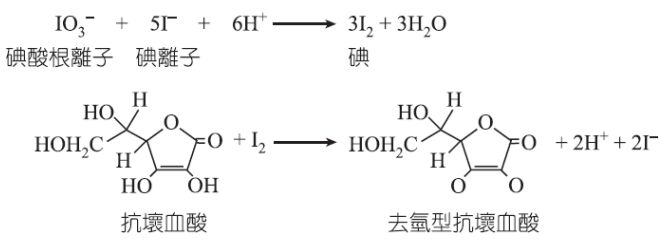
2、:右圖是以鉛蓄電池電解 NaOH(aq)及 KI(aq),A、B、C、D 均為 Pt電極甲為 10g 10%之 NaOH(aq)乙為 2 升 1M 之
KI(aq)。在 25°C 1atm 通電 32 分 10 秒,若電鍍為 10A,則: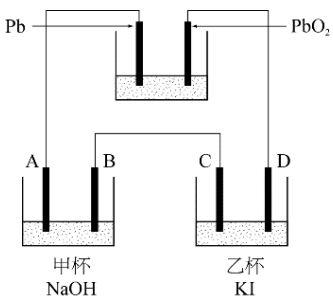
7. PCl5 的分解反應為 PCl5(g) PCl3(g)+Cl2(g),於某溫度時,在體積 V 的平衡系中 PCl5 有 50% 解離。於同
溫下,將體積增為 2V,則 PCl5 有若干 % 解離?(
PCl3(g)+Cl2(g),於某溫度時,在體積 V 的平衡系中 PCl5 有 50% 解離。於同
溫下,將體積增為 2V,則 PCl5 有若干 % 解離?( =2.24)__(25)__
=2.24)__(25)__