試卷測驗 - 110 年 - 110 教育部受託辦理公立高級中等學校教師甄選:化學科#99880-阿摩線上測驗
lost剛剛做了阿摩測驗,考了15分
1. 在25℃時,溶液中含[H2CO3]=0.10M,  ,則在不發生PbCO3沉澱的條件
下,求溶液中最小的
,則在不發生PbCO3沉澱的條件
下,求溶液中最小的  為若干M?[其中H2CO3的
為若干M?[其中H2CO3的  ,
,  ,
PbCO3的
,
PbCO3的  ]
]
(A) 
(B) 
(C) 
(D) 
2. 蔗糖水解之反應速率常數單位為  ,0.44M蔗糖水溶液在酸的催化下,經過8hr測得有
25%發生水解,當溶液中三種糖的濃度均相同時,約需經過多少 hr?(log2=0.30,
log3=0.48)
,0.44M蔗糖水溶液在酸的催化下,經過8hr測得有
25%發生水解,當溶液中三種糖的濃度均相同時,約需經過多少 hr?(log2=0.30,
log3=0.48)
(A)4
(B)16
(C)20
(D)32。
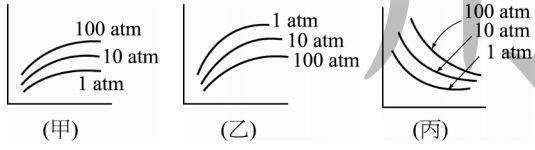
4. 下表有關在 1 大氣壓及 20℃時,不同氣體的密度與溶解度。 
下列敘述,何者不正確?
(A)甲氣體最適宜用來集氣法為 
(B)乙氣體的分子量為 31.2 g/mol
(C)同溫同壓下,若將氣體在 1 升水中長時間的接觸,水中重量以丙氣體增加最多
(D)同溫下,若壓力變為 2 大氣壓時,在 100mL 的水中可溶解氣體丁 176mL。
 (尚未平衡)
取 100 克含有亞硝酸鈉的樣品,溶於稀硫酸中,以 0.01M 的過錳酸鉀溶液進行滴
定,共用去 12mL。試求原樣品含 NaNO2 約多少 ppm?(式量 NaNO2=69)
(尚未平衡)
取 100 克含有亞硝酸鈉的樣品,溶於稀硫酸中,以 0.01M 的過錳酸鉀溶液進行滴
定,共用去 12mL。試求原樣品含 NaNO2 約多少 ppm?(式量 NaNO2=69)
8. 已知 27℃時  的平衡常數
的平衡常數  ,在 27○C 下,24.6 升的 N2O4
與 NO2 混合氣體平衡時,總壓力為 1.5 atm,若 x 為 NO2 與 N2O4 的莫耳數比值,則
x 值為何?
,在 27○C 下,24.6 升的 N2O4
與 NO2 混合氣體平衡時,總壓力為 1.5 atm,若 x 為 NO2 與 N2O4 的莫耳數比值,則
x 值為何?
(A)0.5
(B)1.0
(C)2.0
(D)4.0。
9. 無水硫酸鈣(CaSO4,式量為 136)固體可作為除濕劑,在 300 K 其平衡反應式與平衡
公
常數(Kp)如下:  ,Kp=2500。
已知 300K 時純水的飽和蒸氣壓為 0.040 atm。在 300K 時,將 1.8 克水及 4.08 克(即
0.03 莫耳)的無水硫酸鈣固體一起放入 30 公升之乾燥密閉容器中,假設 CaSO4.2
,Kp=2500。
已知 300K 時純水的飽和蒸氣壓為 0.040 atm。在 300K 時,將 1.8 克水及 4.08 克(即
0.03 莫耳)的無水硫酸鈣固體一起放入 30 公升之乾燥密閉容器中,假設 CaSO4.2
 不釋放水蒸氣 , 則容器內之相對 濕度可達多少 % ?
不釋放水蒸氣 , 則容器內之相對 濕度可達多少 % ?
(A)41%
(B)63%
(C)82%
(D)100%。
12. 用 200 毫升的蒸餾水洗滌 1.66 克的鉻酸銀,若可能損失的最大百分率約為 0.4%,
試推算鉻酸銀的  =?(原子量:Ag=108,Cr=52)
=?(原子量:Ag=108,Cr=52)
(A) 
(B) 
(C) 
(D) 

二、複選題
14. 將 0.2 莫耳弱酸 HA 和 0.08 莫耳 NaOH,混合後,加水稀釋至 1 升。則下列敘述哪些
B 正確?(log2=0.3)
(A)假如此溶液之 pH=5.0,則此弱酸的 
(B)此
D 溶液為 HA 與 NaA 之緩衝溶液
(C)若繼續加入 NaOH 至當量點,則溶液的 pH 值變
為 7
(D)再加入 0.02 莫耳 NaOH,可得最佳之緩衝效果。
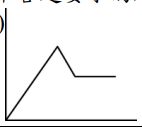
15. 一容積可變的容器內,在 27 ℃ 量得水蒸氣壓變化如附圖所示。在 1 升時,容器中
B 再裝入 N2 氣體 600 mmHg,則下列哪些為正確的敘述? 
(A)容器中水總量約為 0.26 克
(B) 15 升時總壓力為 58 mmHg
(C) 3 升時總壓力為
227 mmHg
(D) 3 升時液體水重約 0.18 克。
16. 在 25°C 時,平衡系  之總壓為 latm,體積為 l.0L,在同溫下若此平
D 衡系之體積擴大為 2.0L 時,下列何項敘述錯誤?
之總壓為 latm,體積為 l.0L,在同溫下若此平
D 衡系之體積擴大為 2.0L 時,下列何項敘述錯誤?
(A)混合氣體之平均分子量增加
(B)平衡系之 PV 值變大
(C)平衡系之氣體總壓介於 latm~0.5atm 之間
(D)平衡系
中之紅棕色加深。
17. 影響反應速率常數(k)、平衡常數(K)的因素,整理如下表:  某反應
某反應  ,其中
,其中  依次表示正、逆反應之速率常數,而 K 為平衡常數,若施予下列操作時,
依次表示正、逆反應之速率常數,而 K 為平衡常數,若施予下列操作時,  將成為
將成為  ,下列結果哪些正確?
,下列結果哪些正確? 
(A)
(B)
(C)
(D)
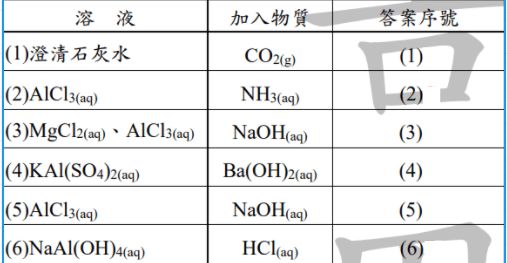
18. A、B 為兩種常見的金屬,依據下列流程加入不同的試劑,會產生以下反應: 
依據此流程回答下列敘述,哪些正確?
(A)Z 的中心原子的混成軌域為 SP3,形狀為正四面體
(B)①~⑥的反應屬於氧化還原的有 3 種,分別是①②③
(C)B 的基態電子組態為[Ar]3d94s2
(D)⑤為加入 K4[Fe(CN)6]產生的反應。
19. 25℃下,有五種混合溶液:① HCl + NaOH ② NaCl + HCl ③ NaOH + H2CO3
④ CH3COOH + CH3COONa ⑤ NaOH + H2SO4 ,其各是以 0.1 M、50 mL 的兩種溶液混合,下列有關此五種溶液的敘述,哪些正確?( log 2 = 0.3 , log3 = 0.48 ,
CH3COOH 的  , H2CO3 的
, H2CO3 的  ,
,  , H2SO4 的
, H2SO4 的  = 極大,
= 極大,  )
)
(A)④可做為緩衝溶液,其 pH 值約為 4.74
(B)反應產物屬於鹼式鹽且為鹼性的為③
(C)反應產物屬於酸式鹽且為酸性的為⑤
(D)②可作為緩衝溶液。
20. 下表為物質甲~戊,在不同溫度時之飽和蒸氣壓(單位:mmHg)。甲~戊皆為共價
B 分子,下列敘述何者正確? 
(A)乙的正常沸點介於 60~80 °C 之間
(B)80 °C 時,若外壓為 1atm,代表乙、丙已經
沸騰
(C)分子間作用力最大者為丙
(D)在正常沸點之下,飽和蒸氣壓的大小關係
為:丙>乙>戊>甲>丁。



4.以下為有機化合物的製造流程:
① 將CH3Br與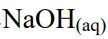 共熱反應產生有機物(甲)。
共熱反應產生有機物(甲)。
②將C2H5OH與酸性之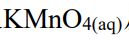 反應產生有機物(乙)。
反應產生有機物(乙)。
③將有機物(甲)與有機物(乙)混合,再加入濃硫酸反應產生有機物(丙)。
④將CH3CH=CH2與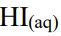 混合反應產生主要產物有機物(丁)。
混合反應產生主要產物有機物(丁)。
⑤將有機物(丁)與NH3反應產生有機物(戊)。
⑥將有機物(丙)與有機物(戊)反應產生有機物(己)和有機物(甲)。
試寫出甲~己有機物的示性式或結構式為何?
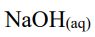 中加熱,使甲完全反應後,將溶液酸化,得兩種主要產物乙及丙。
將乙加入
中加熱,使甲完全反應後,將溶液酸化,得兩種主要產物乙及丙。
將乙加入 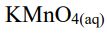 中完全反應後得化合物丁。將丙在鉑黑的催化下做加壓的氫化反應,亦可得
同樣的產物丁。已知丁的分子量為 74。甲、乙、丙、丁為不相同的化合物。試求:
中完全反應後得化合物丁。將丙在鉑黑的催化下做加壓的氫化反應,亦可得
同樣的產物丁。已知丁的分子量為 74。甲、乙、丙、丁為不相同的化合物。試求: