試卷測驗 - 112 年 - 112 高雄市市立高級中等學校聯合教師甄選試題:化學科#114437-阿摩線上測驗
lost剛剛做了阿摩測驗,考了10分
1. 圖 1 為反應速率對時間的變化圖,下列選項中的哪些
反應可用此圖解釋並表示之? 
(A) C(s)+O2(g) ⇌CO2(g),定溫下,壓縮容器體積
(B) 2SO2(g)+O2(g)⇌2SO3(g),定溫下,增加容器體積
(C) 2NH3(g)⇌N2(g)+3H2(g),ΔH=22kcal,定容下,
降低反應時的溫度
(D) H2(g)+I2(g)⇌2HI(g)+2.5kcal,定容下,升高溫度
(E) 2NO2(g)⇌N2O4(g),定溫定容下,再加入NO 與 O2的混合氣體
2. 下列各組物質中,哪幾組可利用加入()內的試劑,來區別分辨出該組的
兩種物質?
(A) 
(B) Zn2+ 、 Al3+ (氨水)
(C) 甘油、乙二醇 (鈉金屬)
(D) 葡萄糖、果糖 (多侖試劑)
(E)  (碳酸氫鈉)
(碳酸氫鈉)
4. 一定溫度下,冰醋酸加水稀釋過程中,溶液的導電度和加入水量的關係如
圖 2,則下列敘述哪些正確?

(A)a、b、c、d 四點,溶液中 pH 值大小:b>a=c>d
(B)a、b、c、d 四點,溶液 pH 值大小:d>a=c>b
(C)a、b、c、d 四點,醋酸解離度最大的是 d
(D)醋酸的酸游離常數於 b 點時達最大值
(E)在 c 點時,溶液中加入少許鹽酸,可使溶液中
[CH3COO-
]减小
7. 如表 1,a、b、c、d、e、f 分別為 0.05 m 及 0.10 m 下,對應的水溶液所測得之凝固點下降度數。若 a/0.05 > d/0.10,則
下列大小比較,何者正確?

(A) b>a=c
(B) c>a>b
(C) d>f>e
(D) a/0.05 > e/ 0.10
(E) c>d
一、霧霾是由多種汙染物共同組成,其中包含細懸浮微粒(PM2.5)、氮氧化物
(NOx)、CO、SO2…等。探究並了解化學反應對於解決霧霾汙染有著相當的重要性。
已知:2SO2(g) + O2(g)⇌2SO3(g) ΔH=-196.6 kJ/mol.
2NO(g) + O2(g)⇌2NO2(g) ΔH=-113.0 kJ/mol.
二、濃度均為 0.10 M、體積為 V0的
AOH 與 BOH 水溶液,分別加水稀
釋至體積 V,溶液 pH 值隨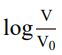 的變化如圖 3 所示,回答下列問題並簡要說明判斷依據:
的變化如圖 3 所示,回答下列問題並簡要說明判斷依據: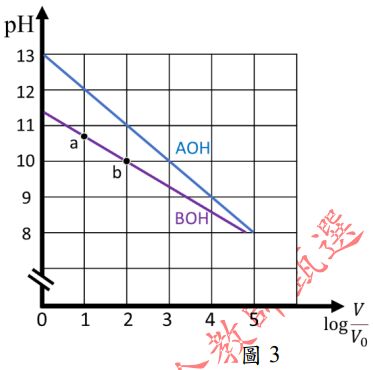
三、有一研發中的生物可降解材料:聚戊二酸丙二酯(Poly ethylene glycol
glutarate,在此簡稱為 PPG),是一種聚酯類,在生物相容性上有很好的發展前景,PPG 其中一種合成的途徑如下方流程圖所示:
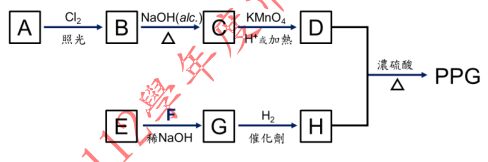
已知:
①化合物 A 為飽和烴,分子量為 70 g/mol.,光譜分析中顯示,碳上所接的
氫皆具有相同的化學環境。
②化合物 B 為一氯取代物,化合物 C 的分子式為 C5H8。
③化合物 E、F 為同系物,分子量恰好相差 14;物質 F 為防腐劑福馬林
(Formalin)的主要成分。
④化合物 G 結構中,僅有一個醛基(−CHO)。
⑤某有機反應: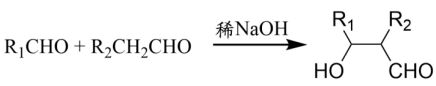
請回答下列問題:
五、在 27℃下,一容器內裝 1atm 氮氣及少量水
(此時水的蒸氣壓及體積忽略不計),並以一
個能自由滑動之活塞(質量不計)構成上、下
兩室(體積分別為 3L、2L),。今將此容器緩
緩加熱至 127℃,上、下兩室體積變化如圖 4
所示,請問原先加入容器的水量為何?(答案求至小數點後一位)(2 分)
1. [方法一]透過已知能量變化的相關程序,推算晶格能,已知:
則 NaCl(s)的晶格能:
Na+
(g) + Cl−
(g)→ NaCl(s) ΔH 晶格 = ? kJ/mol (3 分)
2. [方法二]離子對鍵能推算法:
如圖 5,定 Na+位於立方晶格中心位
置,並令 Na+與 Cl-的鍵距為 r;則由中
心 Na+向外延伸至距離為 r 處有 A 個 Cl
-;距離 處有 B 個 Na+;距離
處有 B 個 Na+;距離  處有 8 個 Cl-;距離
處有 8 個 Cl-;距離 r 處有 6 個
Na+;……依此類推。依據中心 Na+向外延伸時與各層離子間的作用力之總和影響,定出一能量常數 RM如下:
r 處有 6 個
Na+;……依此類推。依據中心 Na+向外延伸時與各層離子間的作用力之總和影響,定出一能量常數 RM如下:
此常數 RM稱為馬德龍常數(Madelung constant),再將馬德龍常數 RM乘
以氯化鈉離子對之鍵能– 492 kJ/mol,即訂為氯化鈉晶體的晶格能。請問:馬德龍常數的推算式中的(A, B)數對為何?(2 分)
十二、 苯環因為 π 電子共振,故相較於烯炔而言,較不易進行 π 鍵的加成反應。當反應在適當的催化劑作用之下,產生親電子基時,此時苯可進行親
電子的取代反應,其反應機制可以用以下流程表示,其中的甲、乙、丙為相關的原子或原子團的代號。請參照流程所示,回答下列問題: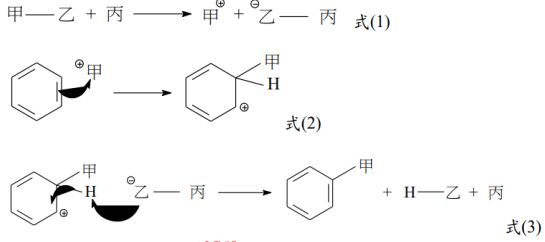
十五、 陳同學在實驗室進行濃度測定實驗,樣品為含有某一元鹼(Kb=10-5 ) 的 未知液,使用酚酞當指示劑,其主要流程如下:
流程1:潤洗滴定管等相關器材。先精秤 KHP,標定出氫氧化鈉標準液的濃度。
流程2:以標定好的氫氧化鈉標準液滴定未知濃度的鹽酸,求出其濃度。
流程3:最後以流程 2 的鹽酸滴定未知液樣品,計算出其濃度。
根據以上實驗流程的敘述,試回答下列問題。
2. 從流程 1 的結果得知:將 0.153 克的 KHP 溶入 20 mL 蒸餾水,達滴定
終點時會耗去 9.38 mL 氫氧化鈉標準液;流程 2 的結果得知:滴定 10
mL 鹽酸時,達滴定終點時會耗去 6.25 mL 氫氧化鈉標準液。流程 3 的
每次滴定操作,未知液體積均為 10 mL,所得數據如表 2: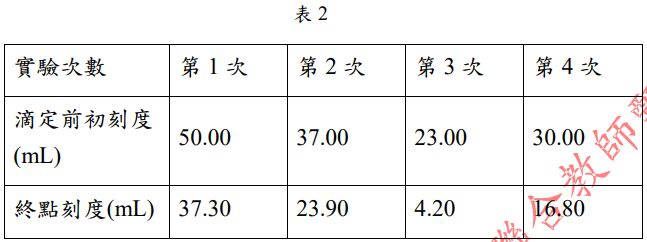 根據上述資料,回答下列問題:
根據上述資料,回答下列問題: