試卷測驗 - 109 年 - 109 大學入學考試中心_指定科目考試:化學#87863-阿摩線上測驗
呂元愷剛剛做了阿摩測驗,考了16分
2. 下列有關化學反應的敘述,哪一項正確? 

(A)反應物粒子只要有足夠的能量,反應就會發生
(B)某一級化學反應在經過一個半生期的時間時,其瞬時反應速率為初始反應速率的一半
(C)圖1為氣體分子運動速率與相對分子數目的分布關係,曲線代表某氣體三種不同溫度,
則高低順序為 T1 > T2 > T3
(D)圖2表示相同的反應物可經由不同反應途徑得到產物A與B。其中,路徑乙的活化能
較路徑甲低,造成兩化學反應差異的原因必為有無添加催化劑
(E)氣態反應中,壓縮反應容器的體積造成濃度增加時,則反應速率必會增加
3-4為題組
無水硫酸鈣( CaSO4 )固體可作為除濕劑,在 300 K 其平衡反應式與平衡常數( Kp)如下:
CaSO4 (s)+ 2 H2O(g)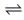 CaSO4● 2H2 O(s) Kp =2500
已知 300 K 時純水的飽和蒸氣壓為 0.040 atm,試回答 3-4 題。( CaSO4 式量為 136)
CaSO4● 2H2 O(s) Kp =2500
已知 300 K 時純水的飽和蒸氣壓為 0.040 atm,試回答 3-4 題。( CaSO4 式量為 136)
3. 在 300 K 時,將足量的 CaSO4●2H2 O(s) 置於一乾燥之密閉容器中,使其達成上述反應之
平衡時,容器內之相對濕度為多少?
(A)30%
(B)40%
(C) 50%
(D) 60%
(E) 70%
4. 在 300 K 時,將 1.8 克水及 x 克的無水硫酸鈣固體一起放入 30 公升之乾燥密閉容器中,
容器內之相對濕度為 82%,則 x 約為多少?(假設 CaSO4● 2H2O(s) 不釋放水蒸氣)
(A)2.0
(B)4.1
(C)5.1
(D) 6.8
(E) 8.2
6. 表 1 是 Mg 2+ 、 Sr 2+ 及 Ba 2+ 三種金屬離子溶液分別與含有 SO42-、CO3 2-及 NH 3 三種試劑
的水溶液反應的結果(所有溶液的濃度均為 0.01M),表中「+」表示有沉澱物生成,「‒」
表示無沉澱物產生。下列各組溶液的成分均為濃度 0.01 M 的水溶液,各自以等體積混
合後,根據表 1,何者不會有沉澱產
生? 
(A) NaOH(aq)與 Mg(NO3)2 (aq)
(B) (NH4 ) 2CO3 (aq) 與 Mg(NO3 )2 (aq)
(C)(NH4 )2 CO3 (aq) 與 Ba(NO3 ) 2(aq)
(D) (NH4 )2 SO4 (aq)與 Sr(NO3)2 (aq)
(E) (NH4)2SO4 (aq)與 Mg(NO3)2(aq)
7. 四種與氧有關的粒子 O3 、 O2 、 O22
- 及 O22+ ,其路易斯結構如表 2 所示。  有關此四種粒子的敘述,哪一項正確?
(甲)臭氧沒有共振結構
(乙)四種粒子中,兩個氧原子間的鍵長是 O22
- > O3 > O2 > O2 2+ (丙)氮氣的電子總數與 O2 2+ 相等
有關此四種粒子的敘述,哪一項正確?
(甲)臭氧沒有共振結構
(乙)四種粒子中,兩個氧原子間的鍵長是 O22
- > O3 > O2 > O2 2+ (丙)氮氣的電子總數與 O2 2+ 相等
(A)只有甲
(B)只有乙
(C)只有丙
(D)甲與乙
(E)乙與丙
9. 感光色素結構的改變啟動了對大腦的神經脈衝,從而形成視覺。而化合物甲為人體視網膜
細胞內之重要感光色素組成的一部
分,化合物甲在吸收光後可轉變為
化合物乙,其分子結構及其光照的轉
換如圖 3 所示。下列關於化合物甲與
化合物乙的敘述,哪一項正確? 
(A)僅化合物甲可與多侖試劑反應,化合物乙則不會反應
(B)化合物甲中的雙鍵均為反式結構
(C)化合物甲中以sp2 混成的碳原子數目有10個
(D)化合物甲與化合物乙分子式相同,具有相同的熔點
(E)化合物甲與化合物乙皆難溶於水,為脂溶性化合物
11. 矽晶( Si)為半導體及太陽能板的重要材料。晶體中的矽原子如金剛石一樣,與鄰近的
四個矽原子以sp3 混成軌域鍵結。若一個矽原子位於圖 4 中正立方
體之中心位置 1 處,則緊鄰此矽原子的其他矽原子的位置為何?
(註:中心位置為 1,其他角落位置為 2–9) 
(A) 2,3,4,5
(B) 2,4,7,9
(C) 2,4,5,7
(D) 3,6,7,9
(E) 3,7,8,9
13. 瑞德西韋是一種曾被試用於治療嚴重特殊傳染性肺炎(COVID-19)患者的藥物,假設
結構如圖 5 所示,則下列有關瑞德西韋的敘述,哪一項正確? 
(A)結構不具有胺類官能基
(B)結構不具有羥基
(C)結構不具醚類官能基
(D)在氫氧化鈉或硫酸水溶液中會被水解
(E)在水中呈弱酸性
14. 合成橡膠常做為汽車輪胎的材料。某一合成橡膠的局部化學結構如圖 6 所示。此合成
橡膠是以化合物甲為單體,彼此透過
一端碳原子進行碳-碳鍵結,如此重複
進行而成的鏈狀聚合物,此過程無其
他副產物生成。試問單體化合物甲的
分子量約為多少? 
(A) 54
(B) 68
(C) 100
(D) 147
(E) 161
15. 物質的狀態變化常伴隨著熱量變化(∆H)。圖 7 是某物質的相圖(未按比例繪製),若
將 100 克此物質置於一體積可變之容器中,則下列
哪一項變化之∆H 會小於 0?  (只考慮相態轉移能量變化)
(只考慮相態轉移能量變化)
(A)在0℃下,由0.5大氣壓降壓至0.3大氣壓
(B)在100℃下,由0.5大氣壓降壓至0.3大氣壓
(C)在0℃下,由1.5大氣壓降壓至0.5大氣壓
(D)在100℃下,由1.5大氣壓降壓至0.5大氣壓
(E)在100℃下,由100.0大氣壓降壓至99.0大氣壓
16. 以鋰金屬為負極材料的鈕扣型電池,具有小而輕、能量密度高以及放電穩定的優點。原
因除鋰的原子量小且為密度最輕的固態金屬性質外,鋰原子的電子組態也是需要瞭解
的環節。而鋰原子的某些電子組態如下:  下列哪一項依序為能量最高和最低的組態?
下列哪一項依序為能量最高和最低的組態?
(A)丙和丁
(B)乙和丁
(C)丙和甲
(D)乙和甲
(E)甲和丁
18-19為題組
一氧化氮和二氧化氮為常見的空氣汙染物。汽機車引擎的高溫可促使空氣中的氮氣與 氧氣反應產生一氧化氮,一氧化氮再與空氣中的氧氣反應產生紅棕色二氧化氮,其反應 式如式(1)所示。兩分子的二氧化氮在密閉系統中可結合生成無色的四氧化二氮氣體, 其反應式如式(2)所示。
2NO(g)+ O2 (g)→NO2 (g) 式(1)
2NO2 (g)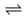 N2 O4 (g) 式(2)
N2 O4 (g) 式(2)
18. 在定溫下,式(1)反應物初濃度( [NO]0 、[O2 ] 0 )與生 成 NO2 之 初速率的關係如表 3
所示。下列相關敘述,哪些正確?

(A)反應物NO的反應級數為1
(B)反應物 O2 的反應級數為1
(C)此反應之速率常數 k 之數值為7000
(D)若 [NO]0 為0.030 M, [O2 ]0 為0.010 M,則
生成 NO2 之初速率為 6.3✖10-2 M/ s
(E)若要改善汽車排放廢氣汙染可加裝觸媒
轉化器,以加快生成 NO2 之速率
19. 在定溫下,測得式(2)的平衡常數( Kc )為 16。下列有關此反應的敘述,哪些正確?
(A)此反應的平衡常數 
(B)反應到達平衡時,容器內顏色雖不再變化,但 NO2 的結合反應與其逆反應仍持續進行
(C)在此溫度下,壓縮系統體積為原有之一半,則平衡會向右移動,導致平衡常數數值
增大
(D)在此溫度下,反應式:  的平衡常數K c = 8 0
的平衡常數K c = 8 0
(E)在此溫度下,反應式:  的平衡常數 K c = 0 25
的平衡常數 K c = 0 25
21. 取一 50 毫升的 0.10 M 醋酸水溶液,以 0.10 M 的氫氧化鈉水溶液進行酸鹼滴定反應。
試問下列敘述,哪些正確?(醋酸的解離常數K a =1.8✖ 10 -5,log2=0.30,log3=0.48)
(A)醋酸水溶液起始的pH值介於0.5 − 1.5之間
(B)此滴定反應,可使用酚酞當指示劑
(C)當加入25毫升的氫氧化鈉水溶液後,該溶液為一緩衝溶液
(D)當加入30毫升的氫氧化鈉水溶液後,溶液的pH值介於3.5 − 4.5之間
(E)當加入50毫升的氫氧化鈉水溶液後,溶液的pH值介於8.5 − 9.5之間
23. 薄荷醇是薄荷油的主要成分之一,其結構式示於圖 8。薄荷醇可由天然薄荷葉片萃取而
得,亦可在實驗室以化合物甲為起始物,經一步反應製得。下列有關此反應、化合物甲
及薄荷醇性質的敘述,哪些正確?

(A)此化學反應過程中,化合物甲被還原
(B)化合物甲的酸性較薄荷醇弱
(C)薄荷醇在適當的條件下,可與二鉻酸鉀溶液反應得到
酮類化合物
(D)薄荷醇中的六員環呈平面結構
(E)化合物甲在氫氧化鈉水溶液的溶解度比在水中的溶解度高
 下列敘述,哪些正確?
下列敘述,哪些正確?
二、氫鍵是一種重要的分子間作用力,除了 H–F、H–O 及 H–N 等鍵結的分子外,還有其他
鍵結方式的分子也會形成分子間氫鍵。例如:H–C≡N 可形成分子間氫鍵,因為氮原子
電負度大,即使間隔一個碳原子,仍可使氫原子帶有部分正電荷而形成氫鍵。氯原子
與氮原子的電負度類似,在某些情況下,含氯的分子也可與鄰近分子的孤對電子(孤
電子對)形成氫鍵。小明在實驗室找了下列四種常見有機物質:甲:正己烷( C6H14 )、
乙:乙醚( C4H 10O )、丙:氯仿( CHCl 3)、丁:2,2-二氯丙烷( C3H6Cl2 )。
將以上物質各取 25.0 毫升於簡易卡計中分別兩兩混合,
達熱平衡後,測量溫度的變化量。當混合後放熱越多,
表示分子間氫鍵越強。依據此一實驗,回答下列問題。
(每一子題 2 分,共 6 分)