複選題
22. 某生在恆溫下進行Na₂S₂O₃水溶液的分解反應速率實驗,反應式如式1:
S₂O₃²⁻ + 2H⁺ → SO₂ + S + H₂O (式1)
其實驗步驟如下:
(a)在一個錐形玻璃瓶中置入50 mL的0.20M Na₂S₂O₃溶液
(b)在瓶子底部下方放置一張畫有黑色「X」標誌的白紙
(c)將10mL的0.10M HCl溶液加入上述錐形玻璃瓶中,並立刻按下秒錶且以玻璃棒攪拌
(d)由錐形瓶開口向下觀察,當無法看見白紙上的「X」標誌時,停止計時並記錄時間(t)
(e)改變步驟(a)的Na₂S₂O₃溶液體積,並另加入適量蒸餾水。再重複上述步驟進行實驗,結果如附表所示:
N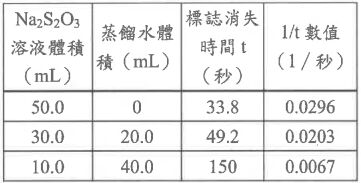
關於實驗結果與推論,下列敘述哪些正確?
(A)此反應對S₂O₃²⁻而言為一級反應
(B)看不清「X」標誌時,代表產生了0.5mmol的硫
(C)看不清「X」標誌是由於產生的二氧化硫氣泡干擾
(D)若將HCl溶液濃度改為0.2M時,不會改變標誌消失的時間(t)
(E)若固定反應總體積,並增加Na₂S₂O₃溶液體積與減少蒸餾水體積,則標誌消失時間(t)將變小
答案:登入後查看
統計: 尚無統計資料
統計: 尚無統計資料