14. 已知反應:2A(g)+B(g) → 3C(g) 為一步驟完成,當 A 為 1 mol,B 為 2 mol 時,反應速率為 R,若改變反應條件,則下列有關速率變化的敘述,何者正確?
(A)定溫、定容下,再加入 2 mol B,則反應速率為 4R
(B)定溫、定容下,再加入 3 mol He,則反應速率為 0.25R
(C)定溫、定壓下,再加入 6 mol He,則反應速率為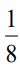 R
R
(D)定溫、定壓下,再加入 6 mol B,則反應速率為 R
R
(E)定溫下,再加入 2 mol B,並將體積擴大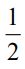 倍,則反應速率為
倍,則反應速率為 R。
R。
答案:登入後查看
統計: 尚無統計資料
統計: 尚無統計資料
詳解 (共 2 筆)
#7301103
首先反應為一單步驟反應,所以其速率定律可直接寫為r=k[A]^2[B]或r=kPA^2PB
(A) 定溫、定容下,再加入 2 mol B,則反應速率=(1^2*4)/(1^2*2) R=2R。
(B) 定溫、定容下,再加入 3 mol He,不影響反應物濃度,故反應速率仍為R。
(C) 定溫、定壓下,再加入 6 mol He,在總壓不變的情況下,分壓改變了,則反應速率=[(1/9)^2*(2/9)]/[(1/3)^2*(2/3)] R=1/27R。
(D) 定溫、定壓下,再加入 6 mol B,在總壓不變的情況下,分壓改變了,則反應速率=[(1/9)^2*(8/9)]/[(1/3)^2*(2/3)] R=4/27R。
(E) 定溫下,再加入 2 mol B,並將體積擴大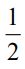 倍,即是在A選項的基礎上使反應物濃度變為2/3倍,則反應速率=2R*(2/3)^3=16/27 R。
倍,即是在A選項的基礎上使反應物濃度變為2/3倍,則反應速率=2R*(2/3)^3=16/27 R。
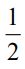 倍,即是在A選項的基礎上使反應物濃度變為2/3倍,則反應速率=2R*(2/3)^3=16/27 R。
倍,即是在A選項的基礎上使反應物濃度變為2/3倍,則反應速率=2R*(2/3)^3=16/27 R。
1
0