19.Biosimilar藥品是大分子藥品,與原廠藥在立體結構上高度相似,下列敘述何者正確?
(A)原廠藥在每一批產品有些微的差異,尤其在製程變動時,也必須證明前後批次藥品高度相似
(B)biosimilar藥品只要以第三期臨床試驗證明與原廠藥相等,就取得許可證
(C)biosimilar藥品在蛋白質第一級至第四級結構都與原廠藥高度相似
(D)biosimilar藥品只有在從未接受過該成分治療的病人可以替代原廠藥
統計: A(1366), B(60), C(154), D(14), E(0) #3378600
詳解 (共 9 筆)
(B) 申請許可證的試驗如下 (不同製劑胰島素、人類生長激素的試驗要求不盡相同,有興趣的同學可參考資料來源)
非臨床試驗: 體外試驗、體內試驗
臨床試驗: 藥動學 (PK) 及藥效學 (PD) 試驗、藥動學及藥效學試驗、藥效學試驗
臨床療效試驗: 比較性療效試驗(試驗的重點在於探討生物相似性藥品與參考藥品間是否具有明顯的療效差異)、臨床安全性和免疫原性評估
Ref: 生物相似性藥品查驗登記基準 衛生福利部 (中華民國113年4月)
(C)(二)原開發廠(參考)藥品與生物相似性藥品的相似與相同:
生物藥大多是蛋白質,蛋白質結構可以分成四級,而生物相似性藥品在第一級結構(氨基酸序列)必須跟參考藥品完全相同。然而在第二級~第四級結構上相似,以整體分子結構而言,生物相似性藥品與原開發藥高度高度相似,但是兩者之治療效果則不具臨床上有意義的差異。
Ref: 台灣生物相似性藥品彙報 (二) Taiwan Biosimilars Update (2)
Derived from : 2025/7/12 https://tsrap.org.tw/medicine_detail.php?id=529
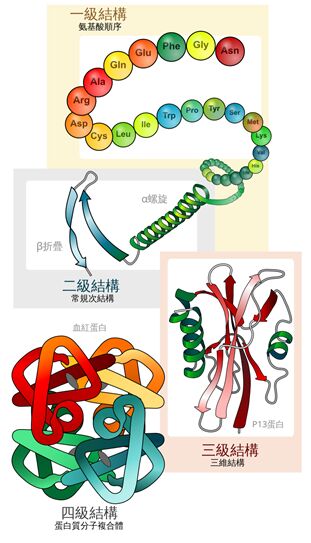
題外話,大家應該還記得,蛋白質的結構分成四級吧! 目前要知道未知蛋白質四級結構的方式有X射線晶體學、核磁共振、低溫電子顯微鏡、去年諾貝爾獎alphafold 所使用的 AI預測。對蛋白質結構和AI有興趣的同學,歡迎來基因體資訊學研究所^_^ 圖ref: https://commons.wikimedia.org/wiki/File:Main_protein_structure_levels_zh_(zh-tw).svg#/media/File:Main_protein_structure_levels_zh_(zh-tw).svg

? 破題關鍵:生物製劑的鐵則——「產品即製程 (The product is the process)」
大分子蛋白質藥物(Biologics)是由「活的細胞或微生物」當作工廠製造出來的。只要是活的生物體,就一定會有不可控的微小變異。
這導致了一個非常重要的結論:即便是「原廠藥自己」,每一批次之間也不可能做到 100% 完美複製! (這跟化學合成的小分子藥物,如普拿疼,可以做到每顆分子結構完全一模一樣是截然不同的)。
因此,當原廠想要更換生產廠房、擴大發酵槽、或改變培養基時,他們自己也必須做一系列的「可比性試驗 (Comparability exercise)」,來向法規單位證明:「我新製程做出來的藥,跟以前舊製程的藥『高度相似』,療效與安全性不變。」 選項 (A) 的敘述完全符合這個生物製劑的基本精神。
? 陷阱大解密:為什麼 B、C、D 都是錯的?
出題老師把法規審查的細節都拿出來當陷阱了,我們一一擊破:
-
❌ (B) 只要以第三期臨床試驗證明與原廠藥相等,就取得許可證?
-
真相: 錯在「只要」這兩個字!生物相似藥的審查講求的是**「整體證據 (Totality of evidence)」**。
-
最核心、也最具決定性的,反而是最基礎的**「分析試驗」(證明理化特性和生物活性高度相似);接著是動物試驗;最後才是為了消除殘存不確定性而做的「臨床試驗」**(通常包含一期 PK/PD 與三期臨床)。絕對不能「只做」第三期臨床就想拿許可證。
-
-
❌ (C) biosimilar藥品在蛋白質第一級至第四級結構都與原廠藥高度相似?
-
真相: 這個陷阱非常細微,考的是生化結構!
-
蛋白質的**「第一級結構(胺基酸序列)」必須是跟原廠藥「完全相同 (Identical)」的!** 不能只是相似。
-
而第二、三、四級結構(立體折疊)以及轉譯後修飾(如醣基化),因為生產的細胞株不同,才允許有微小的差異,達到**「高度相似 (Highly similar)」**。選項統稱第一到第四級都「高度相似」是錯誤的。
-
-
❌ (D) 只有在從未接受過該成分治療的病人可以替代原廠藥?
-
真相: 當然不是!許多國家的法規(包含台灣與美國 FDA)都有明確規範,只要經過嚴格的**「切換試驗 (Switching studies)」,證明病人從原廠藥換成相似藥後,療效不會打折,也沒有增加免疫原性(如產生抗體)的風險,那麼原本就在使用原廠藥的病人,也是可以直接轉換 (Switch) 成生物相似藥的**。
-
? 考場萬用速記總結:
遇到大分子生物藥與 Biosimilar,請在腦中記住這個生動的對比: ? 小分子學名藥 (Generics):像是「影印機」。 可以印出 100% 一模一樣的文件。 ? 生物相似藥 (Biosimilars):像是「畫家臨摹」。 就算請同一個畫家(原廠)畫兩幅向日葵,筆觸也會有些微不同(批次差異);如果是另一個大師來臨摹(相似藥廠),他可以畫到**「高度相似」**,但絕對無法 100% 相同。