4. 根據以下方程式
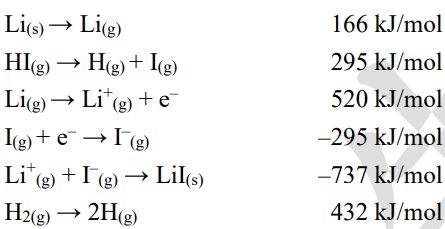
計算以下方程式的焓變化。
2Li(s) + 2HI(g) → H2(g) + 2LiI(s)
(A) 330 kJ
(B) –534 kJ
(C) –483 kJ
(D) 984 kJ
統計: A(3), B(75), C(10), D(9), E(0) #3506526
詳解 (共 2 筆)
題目解析:2Li(s) + 2HI(g) → H2(g) + 2LiI(s) 的焓變化
本題使用 赫斯定律 (Hess's Law),將已知反應式調整係數與方向後相加,即可求得目標反應的焓變化。
1. 調整各項反應式與能量:
• 鋰的昇華: 目標需要 2 莫耳 Li(s),將式 1 乘以 2。
2Li(s) → 2Li(g) ΔH = 166 × 2 = +332 kJ
• 碘化氫分解: 目標需要 2 莫耳 HI(g),將式 2 乘以 2。
2HI(g) → 2H(g) + 2I(g) ΔH = 295 × 2 = +590 kJ
• 鋰的游離: 將 2 莫耳鋰原子轉為離子,將式 3 乘以 2。
2Li(g) → 2Li+(g) + 2e- ΔH = 520 × 2 = +1040 kJ
• 碘的電子親和力: 將 2 莫耳碘原子轉為離子,將式 4 乘以 2。
2I(g) + 2e- → 2I-(g) ΔH = -295 × 2 = -590 kJ
• 晶格能形成: 產生 2 莫耳 LiI(s),將式 5 乘以 2。
2Li+(g) + 2I-(g) → 2LiI(s) ΔH = -737 × 2 = -1474 kJ
• 氫氣形成: 目標產物是 H2(g),給出的式 6 是分解,故需反轉反應方向。
2H(g) → H2(g) ΔH = -432 kJ
2. 加總計算:
將上述調整後的能量全部相加:
ΔH = (+332) + (+590) + (+1040) + (-590) + (-1474) + (-432)
計算過程:
• 注意到 +590 與 -590 相互抵消。
• ΔH = 332 + 1040 - 1474 - 432
• ΔH = 1372 - 1474 - 432
• ΔH = -102 - 432
• ΔH = -534 kJ
結論:
該反應的焓變化為 -534 kJ,正確選項為 (B)。