題組內容
(十二) 實驗的溫度是30.00℃,電化學電池包含一個氫半電池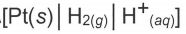 ,是由一個白金電極浸於緩衝溶液中,並處在 某一壓力的氣之下,此氧半電池再连接至另一半電池,由一金屬片(M)浸於未知濃度的
,是由一個白金電極浸於緩衝溶液中,並處在 某一壓力的氣之下,此氧半電池再连接至另一半電池,由一金屬片(M)浸於未知濃度的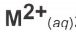 溶液,兩個半電池是由 鹽橋連接如下圖所示。
溶液,兩個半電池是由 鹽橋連接如下圖所示。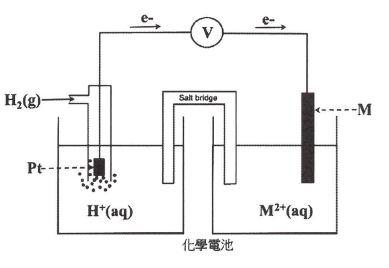
2。電池液中的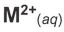 濃度可利用碘滴定法分析,取25.00mL的溶液置於形瓶中, 並加入過量的KI後,產生沉澱物,並需用25.05mL 0.800 M的硫代硫酸鈉溶液滴定方可達當量點,請寫出:
濃度可利用碘滴定法分析,取25.00mL的溶液置於形瓶中, 並加入過量的KI後,產生沉澱物,並需用25.05mL 0.800 M的硫代硫酸鈉溶液滴定方可達當量點,請寫出:
(2)並計算電池液中的 濃度為多少M?(寫到小數點後2位)(2分)
濃度為多少M?(寫到小數點後2位)(2分)
(十二) 實驗的溫度是30.00℃,電化學電池包含一個氫半電池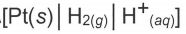 ,是由一個白金電極浸於緩衝溶液中,並處在 某一壓力的氣之下,此氧半電池再连接至另一半電池,由一金屬片(M)浸於未知濃度的
,是由一個白金電極浸於緩衝溶液中,並處在 某一壓力的氣之下,此氧半電池再连接至另一半電池,由一金屬片(M)浸於未知濃度的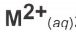 溶液,兩個半電池是由 鹽橋連接如下圖所示。
溶液,兩個半電池是由 鹽橋連接如下圖所示。
2。電池液中的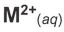 濃度可利用碘滴定法分析,取25.00mL的溶液置於形瓶中, 並加入過量的KI後,產生沉澱物,並需用25.05mL 0.800 M的硫代硫酸鈉溶液滴定方可達當量點,請寫出:
濃度可利用碘滴定法分析,取25.00mL的溶液置於形瓶中, 並加入過量的KI後,產生沉澱物,並需用25.05mL 0.800 M的硫代硫酸鈉溶液滴定方可達當量點,請寫出:
(2)並計算電池液中的 濃度為多少M?(寫到小數點後2位)(2分)
濃度為多少M?(寫到小數點後2位)(2分)