題組內容
2. 硫離子 S2- 可與許多重金屬陽離子形成沉澱,S2- 的來源可利用通入 H2S 氣體到水溶液中,在酸性條件下,H2S 在水中的飽和濃度為 0.1M,今已知 H2S 溶於水中會有以下反應平衡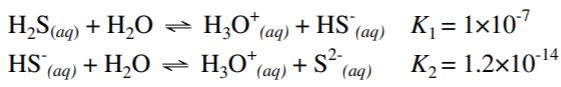
(b) 現有一混和離子溶液含有[Cd2+] 與[Tl+] 各 0.1 M, 假設其 pH=2.0,請問通入 H2S 氣體至飽和濃度可否使其中離子沉澱? 是一種或兩種離子會沉澱 (或沒有沉澱) ? (4 分)
詳解 (共 1 筆)
炘
詳解 #4490610