42.下列何者不是在新藥開發進入臨床試驗前的必備項目?
(A)證明藥效的藥理實驗數據
(B)獲得足量符合品質的原料藥
(C)證明安全性的毒理實驗數據
(D)預測藥物作用的電腦模擬數據
答案:登入後查看
統計: A(556), B(1493), C(220), D(2182), E(0) #3135909
統計: A(556), B(1493), C(220), D(2182), E(0) #3135909
詳解 (共 8 筆)
#6124584
5.下列有關臨床試驗之敘述,何者正確?
(A) 藥品上市前之臨床試驗可分四期(phase 1-4)
(B) 第一期臨床試驗常包括安慰劑組
(C) 第二期臨床試驗必須採用雙盲實驗設計
(D) 第三期臨床試驗為進一步建立藥物之安全性與有效性
ㅤㅤ

ㅤㅤ
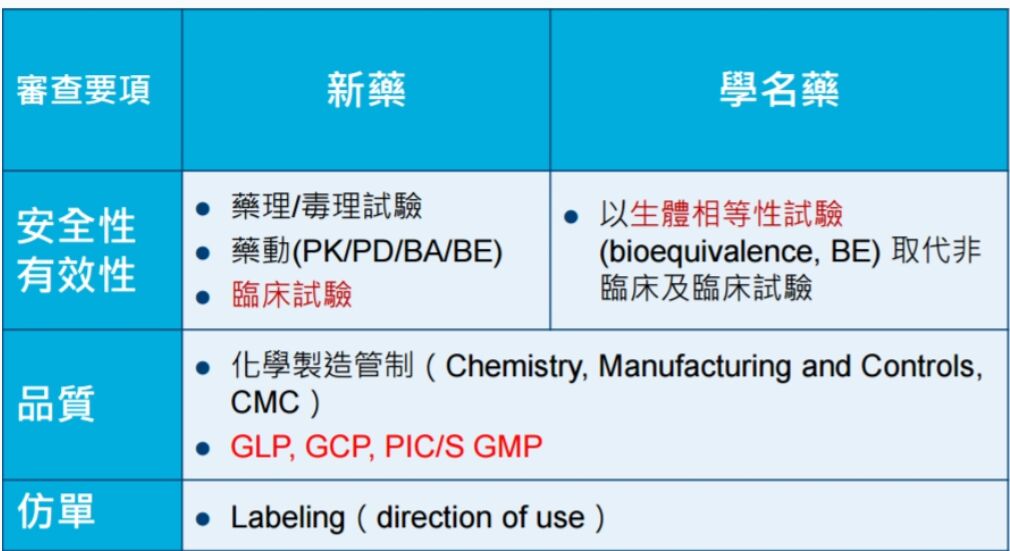
6.下列何者非屬新成分新藥上市前需審查項目?
(A) 藥理/毒理試驗
(B) 吸收、分佈、代謝、排泄試驗
(C) 生體相等性試驗
(D) 臨床試驗
ㅤㅤ
15
0
#6149737
我的想法:
電腦模擬數據只是參考用,不管電腦模擬結果如何還是要實際試驗
「臨床試驗前」就代表準備要試驗了,所以要有足夠的原料藥才可以試驗
13
0
#6612703
一、新藥開發流程簡介
-
藥物發現(Drug discovery)
-
前臨床試驗(Preclinical studies)
-
臨床試驗(Clinical trials)
-
藥證申請與審查(New Drug Application, NDA)
-
上市後監測(Post-marketing surveillance)
二、進入臨床試驗前的「前臨床研究」重點
藥物要從實驗室進入人體試驗(即臨床試驗)前,必須完成以下幾項法規上必要的項目:
1. 藥理作用(Pharmacology)
-
證明藥物對預期適應症具有治療效果。
-
包含 primary pharmacodynamics(主作用)與secondary pharmacodynamics(其他可能的作用)。
-
在細胞、動物模型中測試其活性。
2. 毒理學測試(Toxicology)
確保藥物對人體不會造成過度危害,主要測試包括:
-
急性毒性(Acute toxicity)
-
慢性毒性(Chronic toxicity)
-
致突變性(Mutagenicity)
-
致癌性(Carcinogenicity)
-
生殖毒性(Reproductive toxicity)
毒理數據是送交IND申請的重要核心資料!
3. 原料藥與製劑品質資料(CMC)
-
CMC = Chemistry, Manufacturing, and Controls
-
藥物的來源、生產過程、純度、穩定性等,都需符合GMP或類似標準。
-
為了臨床試驗順利進行,需有「足量且符合規格的原料藥與製劑」。
三、電腦模擬
- 電腦模擬目的為加速藥物設計或預測可能毒性,無法取代實際的體外與動物實驗數據,因此不是法規上的強制要求
四、臨床前階段結束後會進入什麼?
完成上述研究資料後,藥廠會提出:
-
IND申請(Investigational New Drug application)
-
向主管機關(如FDA、TFDA)申請開始第一期臨床試驗
2
0