題組內容
三、酸鹼滴定為實驗室中常用來測定未知物質濃度的實驗技巧,我們可以將未知濃度的酸(鹼)加入錐形瓶中,並滴入適當的指示劑。接著在滴定管中加入適當的鹼(酸),並滴定之,即可藉由解離出的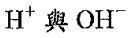 相等來計算未知物的濃度。除了常見的單質子強酸(一元強鹼)滴定一元強鹼(單質子強酸)、單質子強酸(一元強鹼)滴定一元弱鹼(單質子弱酸)之外,二元鹼、二質子酸的濃度與性質亦可藉由滴定做計算與討論。以下討論在50mL的二元鹼 Na2CO3溶液中逐步加入0.1M的單質子強酸HCl,可得到附圖的滴定曲線。
相等來計算未知物的濃度。除了常見的單質子強酸(一元強鹼)滴定一元強鹼(單質子強酸)、單質子強酸(一元強鹼)滴定一元弱鹼(單質子弱酸)之外,二元鹼、二質子酸的濃度與性質亦可藉由滴定做計算與討論。以下討論在50mL的二元鹼 Na2CO3溶液中逐步加入0.1M的單質子強酸HCl,可得到附圖的滴定曲線。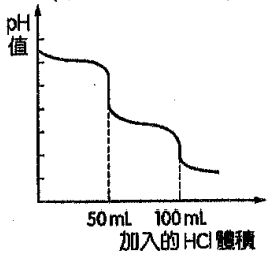
實際上我們可知道,在酸鹼滴定的過程中,溶液依序發生以下的反應:
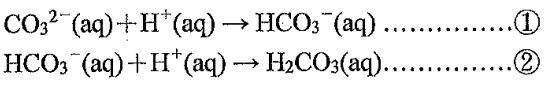
因此曲線中可以發現共有兩個pH值急遽變化的當量點,我們分別稱為第一當量點(50mL處)與第二當量點(100mL處)。藉由兩個當量點的判斷,我們可以知道NasCO)的濃度與各點的pH值。
(1)由此滴定曲線計算,起始的Na2CO3溶液中,Na2CO3 的體積莫耳濃度為多少M?