22.臨床試驗中,受試者發生嚴重不良事件或嚴重藥品不良反應時,下列何者正確?
(A)發生嚴重不良事件時,試驗委託者應立即通知試驗主持人,並儘快提供詳細書面報告
(B)發生未預期嚴重藥品不良反應時,試驗主持人應立即通知人體試驗委員會
(C)發生未預期嚴重藥品不良反應,但若試驗計畫書或其他文件明確排除者,試驗主持人應立即通知執行試驗
之機構
(D)試驗委託者獲知未預期之危及生命之嚴重藥品不良反應,應於獲知日起15日內通報主管機關或其委託機
構,並提供詳細書面資料
統計: A(752), B(4100), C(391), D(1165), E(0) #1740093
詳解 (共 10 筆)
*GCP\藥害救濟\ADR
| 受理機關、團體 | 時限 | 通報 | 通報機關 | 其他 | |
| 藥品優良臨床試驗準則GCP | 人體試驗委員會(保護受試者權利、安全、福祉) | 1個月內完成試驗審查,結果可能是:核准、修正後複審、不核准、中止或終止原核准計畫 | -未預期之死亡或危及生命的嚴重藥品不良反應:7day -未預期之死亡或危及生命以外:15day | 主管機關或其委託機構 | -受試者發生任何嚴重不良事件,試驗主持人應立即通知試驗委託者 -發生未預期嚴重藥品不良反應,試驗主持人應立即通知人體試驗委員會 |
| 藥害救濟法 | 財團法人藥害救濟基金會 | 收受日起3個月內做成審定,得延長1隔月 | x | x | 藥害:因藥物不良反應致死亡、障礙、嚴重疾病 救濟項目:死亡、障礙、嚴重疾病 給付 |
| 嚴重藥物不良反應通報辦法 | X | X | -醫療機構&藥局發現死亡、危及生命:7day -補齊資料&持有該藥物許可證的藥商:15day | 中央衛管機關或其委託機構 |
要注意不良事件跟不良藥品反應 是不同的!
不良事件(跟藥品不以具有因果關係)-- 比較跟藥品無關 故主持人通知委託者就好(感覺比較輕微)
藥品不良反應(有害且未預期、跟藥品有合理因果關係)--有關 主持人要通知 人體試驗委員會!
藥品不良反應--未預期死亡或危及生命 7日內通報 15日補詳細資料
--其他的都15日內(樓上們都有詳細整理)
GCP
1. 臨床試驗 :
(1)符合赫爾辛基宣言
(2)受試者同意書 : 受試者、法定代理人、或有同意權之人於參加試驗前,親筆簽名並載明日期
2. 人體試驗委員會 :
(1)審查受試者同意書、試驗計畫書、及其他相關文件
(2)宜於1個月內完成臨床試驗之審查
(3)定期評估進行中之臨床試驗,每年至少進行1次
(4)保存書面作業程序、委員名單、會議紀錄....等其他臨床試驗相關資料至試驗結束後3年
(5)試驗主持人及試驗機構應保存所有臨床試驗相關之重要文件,至試驗藥品於我國核准上市後至少2年
3.藥品不良反應 :
(1)不良事件 : 試驗主持人→試驗委託者
(2)未預期的嚴重不良反應 : 試驗主持人→人體試驗委員會
(3)死亡或危及生命 : 7天內通報,15天內提供詳細書面資料
(4)死亡或危及生命以外 : 15天內通報
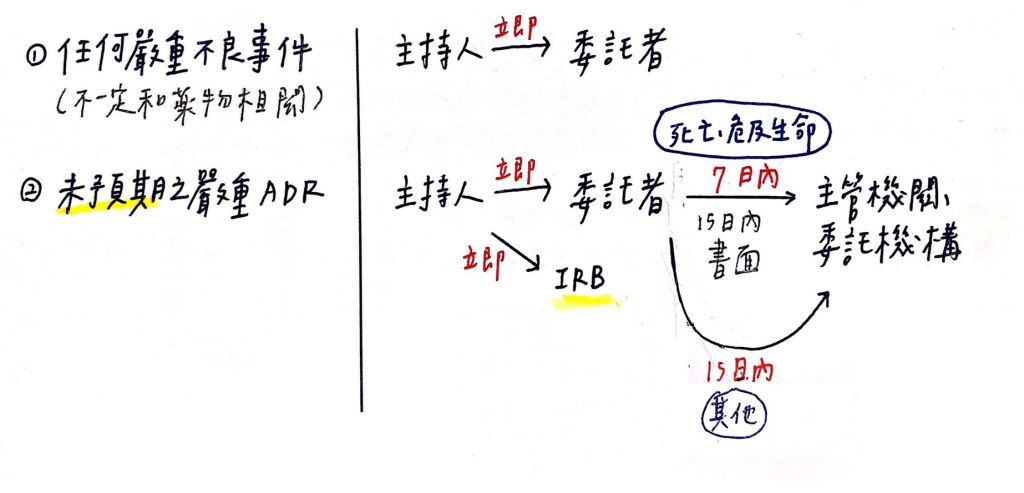
關於未預期之嚴重ADR,主持人通知委託者的時機,應該是立即
(未預期嚴重ADR應該包含在106條提到的"任何嚴重不良事件")
藥品優良臨床試驗準則 第106條
受試者發生任何嚴重不良事件,試驗主持人應立即通知試驗委託者,並儘快提供詳細書面報告。
整題都在考106條~
(A)藥品優良臨床試驗準則 第106條
受試者發生任何嚴重不良事件,試驗主持人應立即通知試驗委託者,並儘快提供詳細書面報告。 <選項內容顛倒了~>
(C)藥品優良臨床試驗準則 第106條
發生未預期之嚴重藥品不良反應,試驗主持人應立即通知人體試驗委員會。但若試驗計畫書或其他文件明確排除者,不在此限。
<不用立即通知> (D)藥品優良臨床試驗準則 第106條
試驗委託者獲知未預期之死亡或危及生命之嚴重藥品不良反應,應於獲知日起七日內通報主管機關或其委託機構,並在獲知日起十五日內提供詳細書面資料。
<分為7天內通報和15天內送書面資料>
補充個名詞解釋
|
|
定義 |
|
|
試驗機構 (Hospital) |
執行臨床試驗之醫療機構 |
執行臨床試驗之醫院層級:必須為教學醫院
|
|
試驗 主持人 (Investigator) |
試驗機構執行 臨床試驗之負責人 |
須為醫師 |
|
試驗 委託者 (Sponsor) |
臨床試驗之 發起及管理者 |
試驗主持人若獨立負起臨床試驗的規劃和所有責任時,則視為試驗委託者 |
|
受託研究機構 (CRO) |
和試驗委託者締約以承擔臨床試驗一部或全部工作之個人或機構 |
|
藥品優良臨床試驗準則 第 106 條 受試者發生任何嚴重不良事件,試驗主持人應立即通知試驗委託者,並儘快提供詳細書面報告。發生未預期之嚴重藥品不良反應,試驗主持人應立即通知人體試驗委員會。但若試驗計畫書或其他文件明確排除者,不在此限。
試驗委託者獲知未預期之死亡或危及生命之嚴重藥品不良反應,應於獲知日起七日內通報主管機關或其委託機構,並在獲知日起十五日內提供詳細書面資料。
試驗委託者獲知未預期之死亡或危及生命以外之嚴重藥品不良反應,應於獲知日起十五日內通報主管機關或其委託機構,並提供詳細書面資料。
第一項之口頭及書面報告,應以受試者代碼代表受試者之身分,不得顯示受試者之姓名、身分證統一編號、住址或其他可辨認受試者身分之資訊。
嚴重不良事件與嚴重藥品不良反應之項目由主管機關公告之。
五樓有點不完整,做點小補充
3.藥品不良反應 :
(1)不良事件 : 試驗主持人→試驗委託者 (立即)
(2)未預期的嚴重不良反應 : 試驗主持人→人體試驗委員會 (立即)
試驗主持人→試驗委託者 (立即)
試驗委託者→主管機關或其委託機構 (期限看第3、4點)
(3)死亡或危及生命 : 7天內通報,15天內提供詳細書面資料
(4)死亡或危及生命以外 : 15天內通報+詳細書面資料
感謝10F我來修正了~